近日,商务部、国家卫健委等12部门联合印发《促进健康消费专项行动方案》,明确将特殊医学用途配方食品(以下简称特医食品)纳入重点发展领域。特医食品作为支持全民健康、促进精准营养消费的重要载体,其产业发展正迎来政策利好窗口。
途配方食品(简称特医食品)是为了满足进食受限、消化吸收障碍、代谢紊乱或特定疾病状态人群对营养素或膳食的特殊需要,专门加工配制而成的配方食品。
特医食品的作用价值
作为精准营养的重要组成部分,其科学设计的配方已在肿瘤治疗、术后康复、罕见病干预、代谢调控等多个临床场景中发挥关键作用。有助于优化医疗资源配置、减轻诊疗负担。面对人口老龄化趋势,特医食品在老年人群慢病管理中的价值更加突出。针对肌肉衰减、吞咽障碍等老年常见问题,特医食品可提供易吸收的营养支持,降低并发症风险。
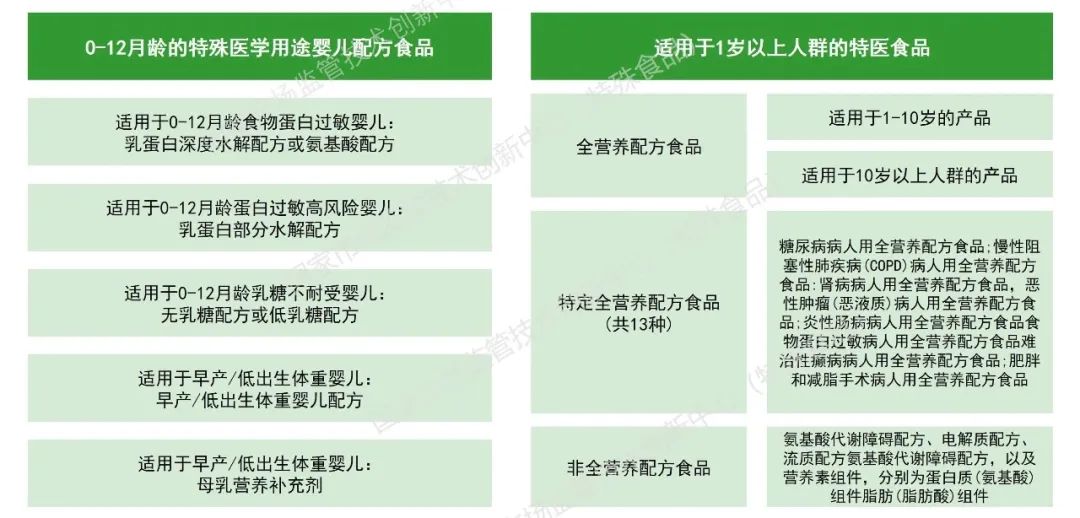
特医食品的难点堵点
特医食品主要消费场景仍集中在医院内,在社区、药店、养老机构等场所的使用和消费明显不足。特医食品在医院信息系统(HIS)中仅以临时编码的形式存在,不便于医生为患者使用;适用于罕见病及临床急需的特医食品较少,患者选择余地不大,且大多为国外产品,国产替代率较低。
此外,公众和专业群体对特医食品的认知水平仍有待提升。在供给端,优质产品数量仍显不足。我国特医食品企业研发基础较为薄弱,注册产品存在同质化现象。
创新监管机制助力特医食品
为实现食品安全监管与产业发展的动态平衡,市场监管总局通过构建“安全筑基、创新驱动、效能提升”三位一体的治理模式,持续推动特医食品产业规范化、制度化发展。
相关负责人介绍,在准入管理方面,市场监管总局以“四个最严”要求为纲领,严格“产品注册+生产许可”双准入控制,修订《特殊医学用途配方食品注册管理办法》,进一步强调申请人应具备的条件、能力、法律责任和义务,明确7种不予注册的情形;正在组织修订《特殊医学用途配方食品生产许可审查细则》,进一步严格生产许可条件,保障特医食品质量安全。
为激活产业创新动能,市场监管总局加强政策支持。建立特医食品分类注册制度,发布电解质配方等多类产品注册指南,优化申报材料;建立优先审评通道,大力压缩适用于罕见病等临床急需特医食品审评时限;先后发布《特殊医学用途配方食品注册临床试验质量管理规范》《特定全营养配方食品临床试验技术指导原则 肝病》等规范指南,积极推动临床急需产品申报上市。
在机制创新方面,市场监管总局联合有关部门推出了一系列新制度安排和支持举措,并通过多部门联动形成政策合力。市场监管总局特殊食品司与国家卫生健康委食品司在特医食品审评审批领域建立“技术联动、专家联审”机制,两部门建立跨学科专家审评团队,实施“常规审评+优先通道”双轨制。对临床急需的罕见病类、特定全营养配方食品等,优先安排审评资源,通过分类管理优化资源配置,加速填补特医食品的供给缺口。
多部门协作也在持续推进中。商务部、国家卫生健康委、市场监管总局等12部门联合印发《促进健康消费专项行动方案》,提出鼓励企业加强工艺研发、产品创新、品质管控,着力发展特医食品。市场监管总局通过强化监管、优化审批、激励研发和多部门协同,引导特医食品生产经营企业主动提供更多优质的健康消费选择。
点击阅读原文

